Возрождение натрий-ионных батарей комнатной температуры
Из-за обильных запасов натрия (Na) в земной коре и схожих физико-химических свойств натрия и лития, электрохимическое хранение энергии на основе натрия имеет значительные перспективы для крупномасштабного хранения энергии и развития сетей. Например, высокотемпературные элементы для исследования батарей с нулевым уровнем выбросов на основе систем Na/NiCl2 и высокотемпературные элементы Na–S, которые являются успешными коммерческими примерами стационарного и мобильного применения, уже продемонстрировали потенциал перезаряжаемых батарей на основе натрия. Однако их высокая рабочая температура, составляющая около 300 °C, вызывает проблемы с безопасностью и снижает эффективность натрий-ионных батарей (SIB). Поэтому SIB, работающие при комнатной температуре (RT), широко рассматриваются как наиболее многообещающая технология, альтернативная LIB.
За последние 200 лет в истории аккумуляторов исследования SIB активно проводились параллельно с разработкой LIB. Электрохимическая активность TiS2 в отношении лития и возможность его хранения энергии были впервые выдвинуты в 1970-х годах. После этого открытия в начале 1980-х годов была реализована способность ионов Na внедряться в TiS+2. С открытием графита как недорогого анодного материала средней емкости для ЛИА и невозможностью интеркалировать ионы натрия в 1990-х годах произошло быстрое развитие ЛИА, превзошедшее рост химии натрия. Затем, в 2000 году, возможность хранения натрия в твердом углероде (HC), который обеспечивал бы энергетическую емкость, аналогичную энергоемкости лития в графите, возобновила исследовательский интерес к SIB.
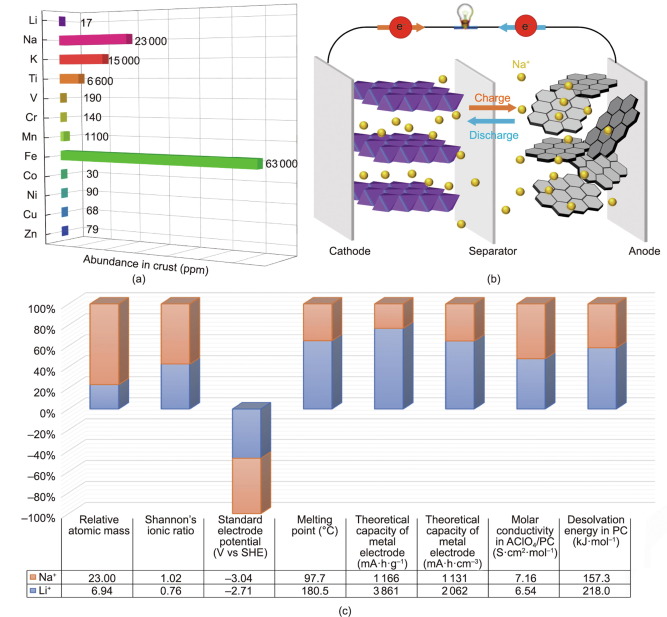
Сравнение натрий-ионной батареи и литий-ионной батареи
Возрождение SIB – в сочетании с постоянно растущим давлением из-за нехватки литиевых запасов и соответствующим ростом стоимости – представляет собой дополнительную стратегию для LIB. SIB привлекают все большее внимание исследователей в сочетании с фундаментальными достижениями в области материаловедения в стремлении удовлетворить растущее проникновение технологий возобновляемой энергетики. Компоненты ячеек и механизмы электрохимических реакций СИБ в основном идентичны компонентам ЛИА, за исключением носителя заряда, которым в одном является Na, а в другом - Li. Основная причина быстрого расширения химии материалов СИБ связана с параллелями в физико-химических свойствах двух щелочных металлов.
Во-первых, принципы работы и конструкция ячеек SIB аналогичны коммерческим LIB, хотя в качестве носителя заряда используется Na. В типичном СИБ существуют четыре основных компонента: катодный материал (обычно Na-содержащее соединение); анодный материал (не обязательно содержащий Na); электролит (в жидком или твердом состоянии); и сепаратор. В процессе зарядки ионы натрия извлекаются из катодов, которые обычно представляют собой слоистые оксиды металлов и полианионные соединения, а затем вводятся в аноды, в то время как ток проходит через внешнюю цепь в противоположном направлении. При разрядке Na покидает аноды и возвращается в катоды в процессе, называемом «принципом кресла-качалки». Эти сходства позволили предварительно понять и быстро развить технологию SIB.
Более того, больший ионный радиус Na имеет свои преимущества: повышенную гибкость электрохимической положительности и снижение энергии десольватации в полярных растворителях. Больший зазор в ионном радиусе между ионами Li и ионами переходных металлов обычно приводит к нарушению гибкости конструкции материала. Напротив, система на основе натрия обеспечивает более гибкие твердые структуры, чем система на основе лития, и обладает огромной ионной проводимостью. Типичным примером является β-Al2O3, для которого интеркаляция Na имеет идеальный размер и высокую проводимость. Более слоистые оксиды переходных металлов с различными способами укладки M+x+ можно легко реализовать в системе на основе натрия. Точно так же широкое разнообразие кристаллических структур, известных для семейства натриевых ионных проводников (NaSICON), намного сложнее, чем у литиевых аналогов. Что еще более важно, в соединениях NaSICON может быть разрешена гораздо более высокая ионная проводимость, которая намного превышает ионную проводимость соединений литий-ионного проводника (LiSICON).
И последнее, но не менее важное: систематические исследования с различными апротонными полярными растворителями показали, что больший ионный радиус Na вызывает меньшую энергию десольватации. Меньший Li имеет более высокую плотность поверхностного заряда вокруг ядра, чем Na, когда оба имеют одинаковую валентность. Таким образом, Li термодинамически стабилизируется за счет совместного использования большего количества электронов с молекулами полярного растворителя. То есть Li можно отнести к разновидности кислот Льюиса. В результате для сильно поляризованного Li требуется относительно высокая энергия десольватации, что приводит к относительно большому сопротивлению переноса, индуцируемому транспортом Li из жидкого состояния (электролита) в твердое состояние (электрод). Поскольку энергия десольватации тесно связана с кинетикой переноса, происходящей на границе раздела жидкость/твердое тело, относительно низкая энергия десольватации является существенным преимуществом для создания мощных СИБ.